俗话说病从口入,吃下去的病可真不少。除了三高等等代谢相关的疾病,不少传染病也是吃出来的。毕竟对各种病原体来说,消化道里娇弱的粘膜可比皮肤好突破多了,甲肝、霍乱等等,都是通过消化道传播。就连最近这个新型冠状病毒,也被发现存在消化道传播的可能。
为了应对这些病原体的入侵,我们的肠道粘膜里驻守了大量的免疫细胞。但过强的免疫不但浪费,本身也会对身体造成损伤。幸好我们的身体非常聪明。
近日,澳大利亚沃尔特和伊丽莎霍尔医学研究所的Cyril Seillet 和Gabrielle Belz等研究发现,小鼠肠道里的固有免疫功能,会在一天中波动,在每天该吃饭的时候增强,进食后还会进一步增强,预防可能发生的感染,其它时间则保持一个较低的水平,避免免疫过度激活的副作用。这一研究发表在Nature Immunology上[1]。
人是铁饭是钢,一顿不吃饿得慌。只是这饭里除了有各种营养外,还可能有着各种病原体。吃了不干净的东西后上吐下泻、胃肠绞痛的经历,估计不少人都有过。
为了应对食物中可能存在的种种病原体,肠粘膜里有着不少免疫细胞驻守,比如先天淋巴细胞(ILCs),尤其是其中的ILC3亚群,一面杀死病原体,一面分泌细胞因子招募免疫细胞[2]。它所分泌的IL-22还作用到肠粘膜上皮,维护粘膜的屏障功能,促进损伤修复,应对细菌感染等造成的炎症[3,4]。
但要是ILC3过于活跃,持续地分泌IL-22,免疫反应太过强烈,却也会导致肠道的慢性炎症,破坏屏障功能,增加炎症性肠病的风险,甚至还会增加肠癌的风险[5-7]。
既要最大程度的保护肠道,抵御病原体入侵,又要避免ILC3过度激活的种种副作用,对它活跃程度的调节就十分重要了。至于机体是怎么调节ILC3活性的,研究人员第一个想到的就是昼夜节律。
研究人员把小鼠养在了一个严格控制光照周期的环境里,每天开始光照的时间记为t0,12小时后的t12时结束光照,进入12小时的黑暗。也就是t0~t11这段相当于白天,而t12~t23相当于夜晚。
在这样的环境里,研究人员发现,小鼠肠道中ILC3的IL-22表达,在夜晚的t16时明显高于白天t4时。而其它地方,比如肺和肠系膜淋巴结,其中的ILC3并没有这样的昼夜活动差异。
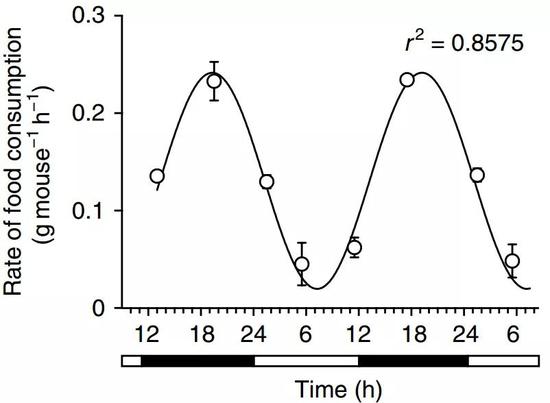
小鼠主要在夜间进食
小鼠是一种夜行动物,在晚上更为活跃,也主要是在晚上吃东西。这样,小鼠夜间进食的同时,ILC3也更为活跃,能更好的抵御食物中潜在的威胁。不过进一步的试验中,研究人员发现,敲除了肠道里的生物钟基因Arntl后,ILC3的昼夜活跃程度差距有所减小,但依然存在。
还有别的调控ILC3的机制。
研究人员接下来限制了给小鼠提供食物的时间,让小鼠只能在白天或晚上进食。这样一周下来,小鼠昼夜节律还没有出现显著变化,但在t4时,相比刚开始吃饭的日间进食小鼠,刚吃过饭的夜间进食小鼠的ILC3明显更为活跃,分泌IL-22的细胞比例多了2倍左右。
而如果把小鼠从t12时开始禁食16小时,直到第二天t4时进行检测,也会让小鼠肠道里的ILC3相比自由进食的小鼠更不活跃,更少分泌IL-22。
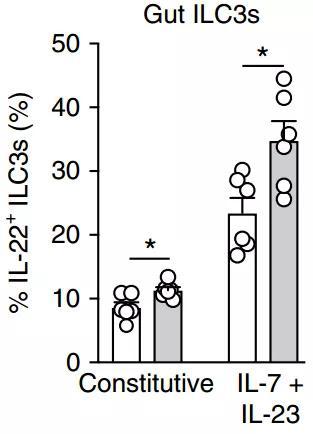
禁食后(白色)小鼠肠道ILC3s中IL-22阳性的比例明显低于自由摄食(灰色)的小鼠
进一步的研究发现,小鼠肠道中的ILC3细胞上有血管活性肠肽(VIP)受体的表达,空间上也和分泌VIP的神经元十分接近。正是进食过程中食物的摄入,刺激了肠神经系统分泌VIP,激活了负责肠道免疫的ILC3细胞。
这样,每天到了该吃饭的时候,肠道免疫就会先在生物钟的作用下预先激活,为迎接食物做好准备。等到真的开始进食后,食物的刺激又让肠道免疫进一步激活,更好防范食物中可能存在的病原体。同时,这也有效地避免了免疫过度激活可能造成的种种问题。
但如果进食规律被打乱,根据生物钟预先上调的免疫就起不了什么作用了。研究人员认为这可能能解释,为什么打乱昼夜节律和进食规律会增加肠道慢性炎症。
虽说这还只是一个小鼠研究,小鼠跟人的进食规律也有很大的差异,但每天按时吃饭总归还是没错的。
接下来,研究打算进一步探究哪些食物能更好的启动这一进食相关的免疫保护作用,开发能更好的产生免疫保护的食谱。
 首页
首页







 营业执照公示信息
营业执照公示信息